Электричество и магнетизм |
Упорядоченный хаосРадий, распадаясь, рождает "эманацию"-радон ("эманация" по-латыни - истечение). Ученые изучили продукты радиоактивного превращения тория и среди них нашли газ, который ничем не отличается от радона. Актиний тоже выделяет "эманацию", и она как две капли воды похожа на радон. Все эти три вида "эманации" различаются только массой их атомов и, добавим, своими радиоактивными характеристиками. Уже не один, а целых три инертных газа претендовали на 86-ю клетку таблицы Менделеева. За короткий срок ученые открыли более 30 самостоятельных радиоактивных веществ. Каждое из них предлагали считать за отдельный элемент. Однако таблица Менделеева располагала лишь восемью свободными клетками. Например, три радиоактивных вещества (их назвали уран-икс, ионий и радиоторий) химически были совершенно неразличимы и не имели никаких отличительных черт по сравнению с обычным торием. На клетку 90 периодической системы обрушилась неожиданная беда. Четыре элемента-близнеца предъявили на нее одинаковые права. Пришлось отказаться от старых представлений, что все атомы данного элемента однородны.  Рис. 3. Явление изотопии свойственно не только радиоактивным, но
и всем прочим элементам таблицы Менделеева. На рисунке показано, как построены
три изотопа первого элемента - водорода: протий, дейтерий (они стабильны)
и тритий (он радиоактивен с периодом полураспада около 12 лет)
"Они неоднородны! - заявил Фредерик Содди в 1913 г. - У каждого радиоактивного элемента может быть несколько сортов атомов. У них одинаковый заряд, они обладают одними и теми же свойствами и отличаются друг рт друга только величиной атомных весов". Такие разновидности атомов Содди назвал изотопами (рис. 3). Это был первый шаг к упорядочению хаоса в представлениях о мире радиоактивных элементов. Все три "эманации" могли спокойно располагаться теперь в клетке 86 периодической системы, нисколько не нарушая ее основы. Так же разместились и изотопы других радиоактивных элементов. Уже в первые годы изучения радиоактивности исследователи пытались выяснить, подчиняются ли разнообразные цепочки радиоактивных превращений какой-то системе, или же они безнадежно запутаны. И здесь понятие об изотопах внесло ясность. Оказалось, что разные цепочки отдельных радиоактивных распадов могут быть сплетены в длинные цепи, у которых есть вполне определенное начало и столь же определенный конец. И все изотопы радиоактивных элементов - звенья той или иной цепи. Эти цепи называют теперь радиоактивными семействами или рядами радиоактивных превращений, а иногда - радиоактивным древом. Корни, из которых произрастают эти "древа", т. е. родоначальники радиоактивных семейств, - это изотопы урана и тория: торий-232, уран-235, уран-238. В' конце длинных цепочек альфа- и бета-превращений находятся устойчивые (стабильные) изотопы свинца (рис. 4, 5, 6). 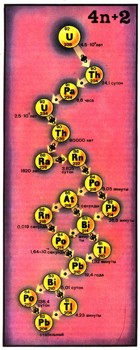 Рис. 4. Радиоактивное семейство урана-238.
Массовые числа всех изотопов, входящих в семейство тория, делятся без остатка на 4. Поэтому то-риевое семейство иногда обозначают как 4n-семей-ство. Аналогичным образом семейства урана-238 и урана-235 будут (4п + 2)- и (4n + 3)-семействами, так как при делении массовых чисел их изотопов на 4 соответственно получается в остатке 2 и 3. 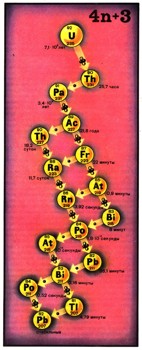 Рис. 5. Радиоактивное семейство урана-235.
Таков был второй шаг, превративший хаос в представлениях о радиоактивных элементах в строгий порядок. Но радиоактивность продолжала загадывать ученым трудные загадки. Ну, скажем, почему не удавалось обнаружить в природе ни одного изотопа, который входил бы в (4n + 1)-семейство? Куда делось это четвертое радиоактивное "древо"? 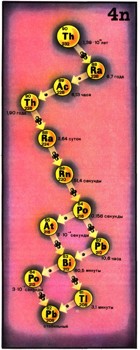
|
 |