Беседа о самом необыкновенном в мире веществе |
Электрохимия в современной науке и техникеВо второй половине XIX в. электрохимические источники тока уступили место электромагнитным генераторам, более удобным для производства электроэнергии в больших масштабах. Но сама электрохимия продолжала развиваться. Появились большие электрохимические производства. С помощью электролиза получали не только водород и кислород, хлор и щелочи, но и металлы — магний и алюминий, в которых нуждаются многие отрасли современной техники. 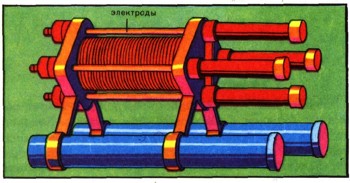 Батарея водородно-кислородных элементов. Мощность ее более 5 кВт. Диаметр каждого электрода 250 мм. С помощью электрохимических методов при анализе химики обнаруживают различные вещества. Существуют электрохимические приборы, которые улавливают и регистрируют звуковые колебания, измеряют давление, ускорение, вибрации и другие разнообразные физические величины. Но электрохимические реакции не всегда приносят пользу. Есть электрохимический процесс, который приводит к неисчислимым убыткам. Это коррозия металлов, уносящая каждый год десятую долю всего выплавляемого железа. Поэтому электрохимики изобретают средства как для ускорения электрохимических реакций, так и для их замедления. Электрохимические реакции удобны тем, что их скорость можно регулировать довольно простыми способами. Это очень важно, когда имеешь дело с несколькими реакциями одновременно. Замедляя одни реакции и ускоряя другие, можно управлять процессами. Поэтому одним из важнейших разделов электрохимической теории стало учение о скорости электрохимических реакций, или электрохимическая кинетика. Эта теория начала развиваться в 30-е годы XX в. Исследование основных законов электрохимической кинетики позволило усовершенствовать важнейшие электрохимические процессы, в том числе и те, которые были присущи первым источникам тока — гальваническим элементам. |
 |