Замечательные явления на границе между телами |
Почему мыла моютМылообразные поверхностноактивные вещества образуют в воде коллоидные растворы: при определенной концентрации несколько десятков молекул или ионов мыла объединяются в агрегаты — мицеллы (рис. 4). Мицеллы имеют шарообразную форму с гидрофильной оболочкой из полярных групп и гидрофобным ядром из углеводородных цепей. С ростом концентрации мицеллы становятся пластинчатыми — прослойки из углеводородных цепей покрыты с обеих сторон полярными группами. Такие пластинчатые мицеллы являются зародышами кристалликов мыла. Пластинчатые мицеллы сцепляются углеводородными цепями крайних молекул в пространственные сетки-каркасы, и раствор, как говорят, структурируется — приобретает свойство упругого твердого тела, напоминающего желе и называемого гелем. Поверхности, покрытые такими мицеллярными адсорбционными слоями в растворах мыл, всегда хорошо смачиваются водой. Этому помогает сильно пониженное поверхностное натяжение воды на границе с воздухом. Именно поэтому одно и то же вещество может в очень малой концентрации делать твердую поверхность гидрофобной, в большей концентрации давать прямо противоположный результат — смачивать водой любую гидрофобную поверхность (рис. 5). 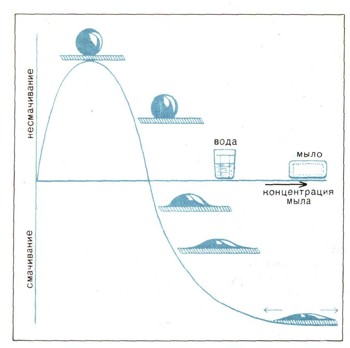 Рис. 5. Влияние адсорбции мыла на смачивание водой твердых поверхностей. Но мыла не только смачиватели; они и сильные стабилизаторы, обеспечивающие устойчивость жидких пленок (вспомним знакомые всем мыльные пузыри) — пен, а также всех дисперсных систем — эмульсий и суспензий. В эмульсиях мелкие капельки одной жидкости, не смешиваясь, распределяются в другой жидкости. Под действием поверхностной энергии они при соприкосновении стремятся слиться друг с другом. Подобно этому сцепляются в агрегаты и частицы твердого тела, образующие суспензию в жидкой среде. Стабилизатор же создает на поверхности капелек эмульсии или частиц суспензии геле-образный (структурированный) адсорбционный слой, который препятствует сближению и взаимодействию частиц. Нальем в стеклянный сосуд (бутылку) воду и, встряхивая, будем понемногу добавлять туда керосин или бензин. Капельки бензина тотчас же начнут сливаться в крупные капли, и смесь разделится на два жидких слоя. Теперь повторим опыт, добавив к воде 1—5 % мыла. При встряхивании образуется молочно-белая устойчивая эмульсия, в которой отдельные капельки, не превышающие сотой доли миллиметра, защищены от слияния адсорбционными оболочками мыла. Водный раствор мыла занимает двадцатую часть сосуда, но его хватает на эмульгирование в 20 раз большего объема бензина, если вводить бензин постепенно, малыми порциями, каждый раз энергично встряхивая. Весь бензин разобьется на мельчайшие капельки, плотно прижатые друг к другу, но устойчиво разделенные тонкими прослойками мыльного раствора. Такие концентрированные эмульсии очень вязки, они напоминают сметану. Кстати, и сметана, и сливки, и молоко — это эмульсии жира в воде, стабилизованные белковым веществом. Попробуем разрезать кончиком стеклянной палочки слой ртути толщиной 2—3 мм, покрывающий дно плоской чашечки или блюдца под водой (рис. 6). Такой разрез сделать нельзя: он тотчас же «залечивается» —смыкается под действием поверхностного натяжения на границе ртуть — вода. Однако, если к воде добавить 1 % сапонина — экстракта из мыльного теория, разрез стабилизируется структурированными адсорбционными слоями. Они примут форму, соответствующую минимуму свободной энергии, которую можно рассчитать математически. Разрез должен кончаться у краев слоя ртути или замыкаться на себя, образуя кружок — кольцо. В одной точке могут пересекаться только три разреза, образуя равные углы в 120°. 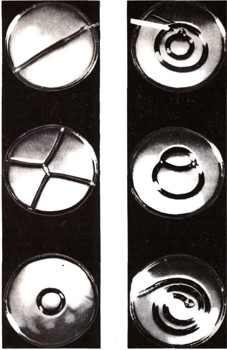 Рис. 6. Формы разрезов слоя ртути, стабилизованных поверхностноактивным веществом. Время жизни таких разрезов возрастает по мере насыщения адсорбционного слоя и характеризует стабилизирующую способность данного поверхностноактивного вещества. Так почему же мыло моет, почему оно легко отмывает с любой поверхности грязь — сажу, масло, нефть? Именно потому, что оно обладает смачивающей и стабилизирующей способностью. Мыло переводит всю грязь в воду в виде тонкодисперсных суспензий и эмульсий. Обычное мыло — натриевые соли жирных кислот — без труда справляется с грязью в мягкой воде, в которой нет солей кальция и магния. В жесткой же воде мыло осаждается в виде нерастворимых кальциевых и магниевых мыл, раствор теряет свою моющую способность. Однако химики создали синтетические мылообразные (моющие) вещества, пригодные для любой воды, даже для морской; особенно хороши неионные мыла, совершенно устойчивые к действию солей. Моющие средства и смачиватели используются в быту, в промышленности и в сельском хозяйстве. Смачиватели применяют при изготовлении фотокинопленки, когда прозрачную полимерную ленту надо равномерно полить светочувствительным составом — высокодисперсной взвесью бромистого серебра на водном растворе желатины. Смачиватель, добавленный в ванну, где окрашивают волокно и ткань, ускоряет процесс и делает окрашивание равномерным. Чтобы избавить шахтеров от вредной пыли, в шахтах распыляют воду с добавкой смачивателя. Пыль улавливается такой водой, и воздух становится чище. Полное смачивание — необходимое условие для взаимодействия жидкости с твердым телом, для проникновения жидкости в тонкие поры. Поэтому-то все ядохимикаты и гербициды, применяемые в сельском хозяйстве, содержат поверхностноактивные вещества. Как выдувать мыльные пузыри Растворите в 100 г теплой дистиллированной или долго кипевшей воды 2 г тонко наструганного сухого детского мыла и 10 г чистого глицерина. Прсле охлаждения к раствору добавьте понемногу крепкого нашатырного спирта, пока раствор не станет прозрачным и не будет сильно пахнуть аммиаком. Затем небольшую стеклянную вороночку, к которой присоединена резиновая трубочка, погрузите раструбом в мыльный раствор. Крупные пузыри хорошо выдувать на блюдце с раствором, смочив им края блюдца. Выдувая пузырь, понаблюдайте, как с уменьшением толщины пленки на ней играют все более и более яркие интерференционные цвета. |
 |